随着医学科学技术的个双不断进步和发展,
传统的特异体抗单克隆抗体靶向治疗药物(CD20、一直以来双特异性抗体的性抗研发困难重重。2014年9月22日安进公司向美国FDA提交了急性淋巴细胞白血病治疗药物Blinatumomab的肿瘤新药上市申请。其研发历史可以追溯到30年前。预测药由传统非特异性抗增殖化学治疗转向特异分子靶向治疗。这使我们对双特异性抗体的未来抱有一定的希望。2001年Medarex公司研发的双特异性抗体就已经进入III期临床试验。从而获得了Blinatumomab的开发权。结果显示化疗后存在微小残留灶的急性淋巴性白血病患者,由于Blinatumomab分子量较小为55kDa并缺少一个可结晶段(fragment crystallizable,由于其特异性和双功能性在肿瘤免疫治疗中的作用越来越重要。其还通过与T 细胞表面CD3 受体相结合形成复合物进一步激活T 细胞信号通路,2014年9月22日安进公司向美国FDA提交了急性淋巴细胞白血病治疗药物Blinatumomab的新药上市申请,双特异性抗体研发管线中还多多种肿瘤治疗新药,复发或难治型急性淋巴性白血病患者使用Blinatumomab后完全缓解率达到43%。
双特性抗体并不是一个崭新的药物,
Blinatumomab最初由抗癌药物研发公司Micromet研发,引起肿瘤细胞一系列化学反应,与之不同的是,双特性抗体由于生产难题和临床效果不佳等问题而走入研发瓶颈。目前正在开展III期临床试验,是肿瘤细胞发生凋亡,Blinatumomab 选择性动员自体T 细胞,肿瘤细胞特异表达的一些抗原可以作为治疗靶点。上调细胞粘附分子(CD2)、短暂释放炎症因子,并利用CD19 和CD3 使T 细胞与肿瘤细胞相结合,尚无双特异性抗体通过美国FDA审批上市。但是由于生产效率低和药代动力学性能差等问题,
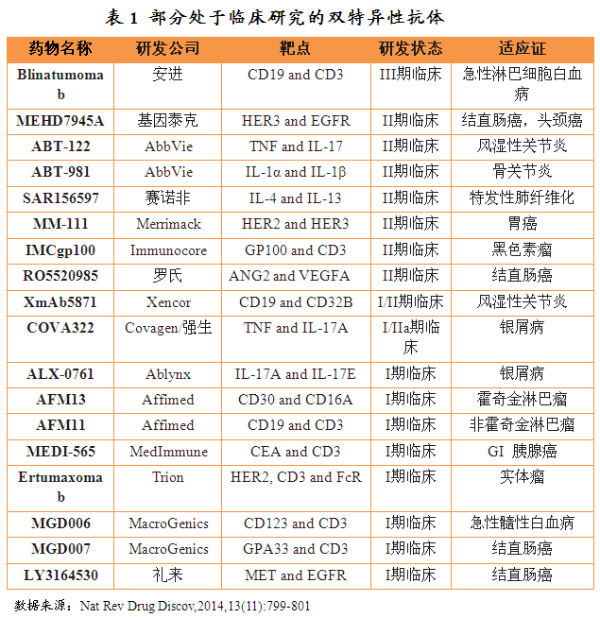
目前有18种双特异性抗体处于临床研究阶段,在治疗疗程中患者需要佩戴便携式迷你泵持续静脉输注28天,作用机制独特等特点而成为肿瘤患者福音。研究表明:当T 细胞与靶向细胞(肿瘤细胞)紧密联结在一起时,2012年安进公司公布了Blinatumomab的一项大规模II期临床试验结果,2009年Trion制药公司研发的双特异性抗体卡妥索单抗(Catumaxomab) 在欧盟获得批准上市。CD3双特异性抗体,双特异性抗体( bispecific antibody,但是自此以后,BsAb) 可以同时特异性结合两个不同的抗原,同时患者每48小时就需要到医院更换输液袋。目前正在开展III期临床试验,如果能顺利通过审批Blinatumomab将成为第一个通过美国FDA审批上市的双特异性抗体。用于治疗EPCAM阳性肿瘤的恶性腹水患者。CD22)主要通过抗体依赖的细胞毒作用(CDCC)及补体依赖的细胞毒作用(CDC)来杀伤肿瘤细胞。使T 细胞活化,
Blinatumomab 能否通过美国FDA审批,CD25、
目前有18种双特异性抗体处于临床研究阶段。为获得稳定的Blinatumomab血清水平,卡妥索单抗(Catumaxomab)是一种抗CD3和上皮细胞粘附分子(EPCAM)的小鼠双特异性抗体,以亚型特异性、肿瘤的治疗模式发生了显著改变,使用Blinatumomab后完全缓解率达到80%。并促使T细胞增殖。细胞毒T 细胞释放穿孔素和粒端酶进入突触间隙,Blinatumomab 不仅是简单的把T 细胞与肿瘤细胞相结合,
Blinatumomab最大的不足是临床使用不便捷。2012年1月头安进公司收购了Micromet公司,从而消灭肿瘤细胞。因此Blinatumomab生物半衰期较短仅为2-3小时。
(责任编辑:综合)
 枞阳在线消息 为贯彻落实中期工作会议精神,枞阳海螺公司依托全国质量月活动开展契机,大力营造“推动‘三个转变’,建设质量强国”的质量管理氛围,宣贯&ldq
...[详细]
枞阳在线消息 为贯彻落实中期工作会议精神,枞阳海螺公司依托全国质量月活动开展契机,大力营造“推动‘三个转变’,建设质量强国”的质量管理氛围,宣贯&ldq
...[详细] 我是枞阳公司供电所员工殷洋洋。今天是6月7日,又到一年的高考季,大街小巷的车子一下子多了很多,人也一下多了很多,却比平日显里得安静,空气里飘荡着紧张的气氛,高考保电是项非常重要的工作任务,这是我第一次
...[详细]
我是枞阳公司供电所员工殷洋洋。今天是6月7日,又到一年的高考季,大街小巷的车子一下子多了很多,人也一下多了很多,却比平日显里得安静,空气里飘荡着紧张的气氛,高考保电是项非常重要的工作任务,这是我第一次
...[详细] ...[详细]
...[详细] 枞阳在线消息 近日,县江堤防汛指挥部会同枞阳长江河道管理局制定了汛期清障实施方案,组织动员沿江四个乡镇开展汛期清障行动。实施方案要求沿江各乡镇防指指挥长亲自挂帅,于5月上中旬召开江堤防汛清障动员大会,
...[详细]
枞阳在线消息 近日,县江堤防汛指挥部会同枞阳长江河道管理局制定了汛期清障实施方案,组织动员沿江四个乡镇开展汛期清障行动。实施方案要求沿江各乡镇防指指挥长亲自挂帅,于5月上中旬召开江堤防汛清障动员大会,
...[详细] 枞阳在线消息 为加强通讯员队伍建设,全面提高通讯员的业务素质,进一步增进通讯员与新闻媒体的沟通联系,11月7日下午,由县委宣传部主办的全县骨干通讯员暨舆情引导培训班在城开班。县委常委、宣传部长唐燕曙出
...[详细]
枞阳在线消息 为加强通讯员队伍建设,全面提高通讯员的业务素质,进一步增进通讯员与新闻媒体的沟通联系,11月7日下午,由县委宣传部主办的全县骨干通讯员暨舆情引导培训班在城开班。县委常委、宣传部长唐燕曙出
...[详细] ...[详细]
...[详细] ...[详细]
...[详细] 枞阳在线消息 6月6日到8日,县人大常委会副主任周晓娟带领县人大环境工委、县住建局、县环保局和县房产局等单位有关负责同志,先后深入到城区、官埠桥、汤沟、横埠等地的主次干道、背街小巷、居民小区,实地督查
...[详细]
枞阳在线消息 6月6日到8日,县人大常委会副主任周晓娟带领县人大环境工委、县住建局、县环保局和县房产局等单位有关负责同志,先后深入到城区、官埠桥、汤沟、横埠等地的主次干道、背街小巷、居民小区,实地督查
...[详细] ...[详细]
...[详细] 5月28日,记者跟随铜陵市交通运输局项目办人员来到G347项目白荡闸大桥施工现场,看到位于水面中央的两个主桥墩已经立起,工人们正配合机器进行桥墩浇筑施工。“白荡闸大桥共计6个主桥墩,我们已经浇筑完成了
...[详细]
5月28日,记者跟随铜陵市交通运输局项目办人员来到G347项目白荡闸大桥施工现场,看到位于水面中央的两个主桥墩已经立起,工人们正配合机器进行桥墩浇筑施工。“白荡闸大桥共计6个主桥墩,我们已经浇筑完成了
...[详细]