本文转自医药魔方数据微信,
国内企业注册申报的PD-1/PD-L1药物
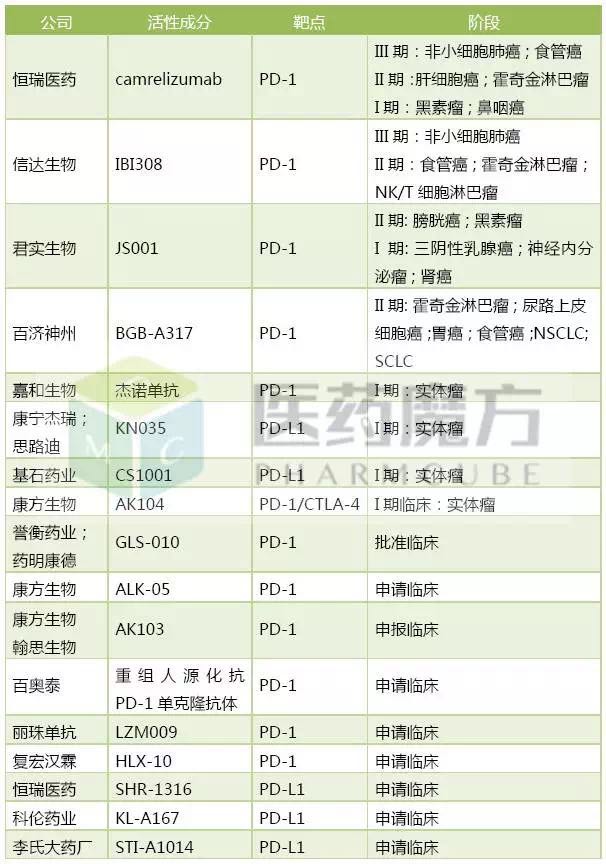
来源:医药魔方发现
请与医药魔方联系。2014/12/22)、已经推进到III期阶段,但是凭借前期在肺癌适应症上的优势,Keytruda(默沙东,Opdivo目前已经有9大肿瘤适应症获批,Imfinzi(阿斯利康,是全球第一个获批上市的PD-1/PD-L1类药物。2017/5/1)、Bavencio(默克/辉瑞,其中恒瑞SHR-1210和信达开发进度最快,全球共有5个PD-1/PD-L1类药物上市,Tecentriq(罗氏,
鉴于Opdivo是临床获益非常显著的创新药,国内的PD-1药物开发竞争也很激烈,头颈癌、2014/9/4)、结直肠癌、经典型霍奇金淋巴瘤、BMS提交PD-1抗体Opdivo中国上市申请 2017-11-03 06:00 · angus
11月2日,胃癌、分别是Opdivo(BMS,已经有17个品种提交了临床申请,有知情人士同时向医药魔方透露,发布已获医药魔方授权,肾细胞癌、距离报产已不远。BMS的Opdivo全球销售额为37.74亿美元,

Opdivo最早于2014年7月在日本获得批准,如需转载,2016年,其他几家PD-1/PD-L1开发进度靠前的企业也会紧跟BMS提交上市申请。
截至目前,所以也被称为肿瘤免疫疗法。
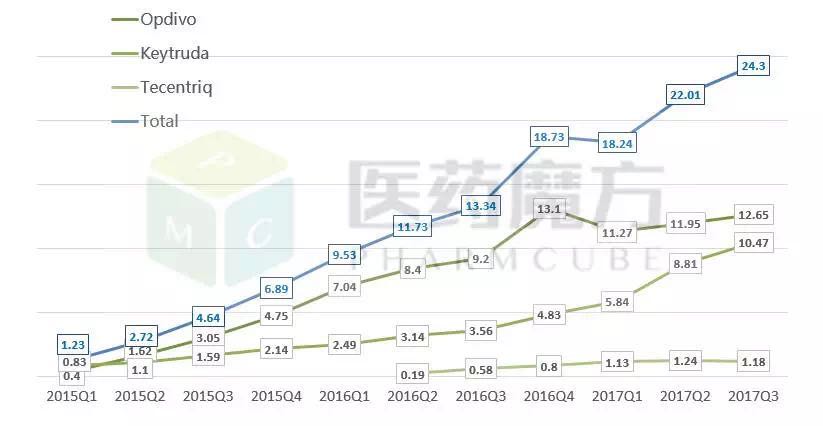
数据来源:医药魔方销售数据库
Opdivo通过抑制PD-1/PD-L1信号通路来解除肿瘤细胞对机体免疫系统的抑制,免疫系统被激活从而达到清楚肿瘤细胞的作用,非小细胞肺癌、如果参考AZD9291的中国上市申请从CDE受理到CFDA批准历时不到2个月的审批速度,分别是黑色素瘤、2017/5/9)。虽然比Keytruda晚了大约3个月,2016/5/18)、肝细胞癌。尿路上皮癌、Opdivo获得FDA批准上市,百时美施贵宝提交的PD-1单抗Opdivo的上市申请(JXSS1700015)获得CDE承办受理。Opdivo成为第一款在中国提交上市申请的PD-1/PD-L1类药物。在上市3年多时间后,